
根据损伤轻重程度不同,分为可复性损伤和不可复性损伤两大类,变性一般为可复性损伤,而细胞死亡则为不可复性损伤。
变性(degeneration)系指细胞或间质内出现异常物质或正常物质的量显著增多,并伴有不同程度的功能障碍。
(一)水变性(细胞水肿)
当缺氧、毒性物质损及线粒体内ATP产生时,细胞膜上的钠泵功能降低,使细胞膜对电解质的主动运输功能发生障碍,更多的钠、钙离子和水进入细胞内,而细胞内钾离子外逸,导致细胞内水分增多,形成细胞肿胀,严重时称为细胞的水变性(hydropic degeneration)。
病理变化 光镜下水样变性的细胞体积增大, 因胞浆内水分含量增多,变得透明、淡染,甚至出现空泡,可称为空泡变性,严重时胞核也可淡染,整个细胞膨大如气球,称气球样变性。常见于心、肝、肾等实质性器官。
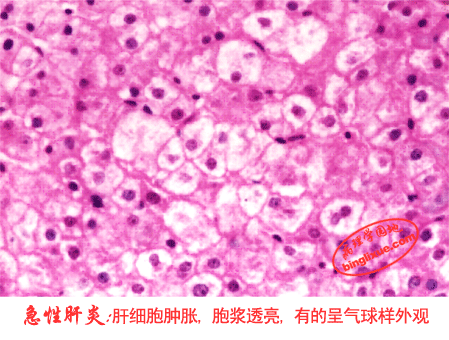
受累脏器肿胀,边缘变钝,苍白而混浊,光镜下胞浆呈粉染细颗粒状,透明度也降低。电镜下内质网和线粒体扩张呈空泡状。
一般而言,细胞水肿是一种可复性的损伤,但是,严重的细胞水肿也可发展为细胞死亡。
(二)脂肪变性
正常情况下,除脂肪细胞外的实质细胞内一般不见或仅见少量脂滴。如这些细胞中出现脂滴或脂滴明显增多,则称为脂肪变性(fatty degeneration)或脂肪变(fatty change)。
脂滴的主要成分为中性脂肪,也可有磷脂及胆固醇等。脂肪变性主要见于肝、心、肾等实质器官,因肝是脂肪代谢的重要场所,帮肝脂肪变性最常见。脂肪变性时最初形成的脂滴很小,以后可逐渐融合为较大脂滴,此时常无界膜包绕而游离于胞浆中。
(1)肝脂肪变性
肝脏的脂肪变性与肝脏的脂肪代谢紊乱有关。肝脏的脂肪代谢过程中的任何一个环节发生障碍,均可造成肝细胞的脂肪变性:①脂蛋白的合成发生障碍:②中性脂肪合成过多③脂肪酸氧化障碍。
病理变化 轻度脂肪变性,肝脏可无明显改变。如果脂肪变性弥漫而严重时,肝脏可明显肿大,色变黄,触之有油腻感称为脂肪肝(fatty liver)。光镜下早期肝脂肪变性,可表现为在肝细胞核周围出现小的脂肪空泡。以后随着脂肪变性的加重,空泡逐渐变大,分布于整个胞浆中。严重者融合成一个大泡,将细胞核挤向一边,形态与脂肪细胞类似。肝淤血时,小叶中央区缺血较重,因此脂肪变性首先在中央区发生。磷中毒时,肝脂肪变性首先发生在小叶周边部,然后,累及整个肝小叶。
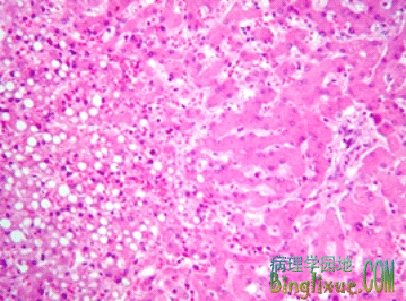
(2)心肌脂肪变性
发生脂肪变性时,心肌细胞内脂滴含量显著增多。心肌脂肪变性最显著的发生部位是乳头肌和心内膜下心肌。重者呈黄*色条纹,轻者呈暗红色,两者相间排列,状似虎皮,故称为“虎斑心”。光镜下脂肪变性的心肌细胞浆中出现细小、串珠样脂肪空泡,排列于纵行的肌原纤维间。
(三)玻璃样变性
玻璃样变性(hyaline degeneration)又称透明变性,系指在细胞内或间质中,出现均质、半透明的玻璃样物质,在HE染色切片中呈均质性红染。它可以发生在结缔组织、血管壁,有时也可见于细胞内。
1. 结缔组织玻璃样变性
常见于纤维瘢痕组织内。肉眼形态:灰白、半透明状,质地坚韧,缺乏弹性。光镜下,纤维细胞明显变少,陈旧的胶原纤维增粗并互相融合成为均质无结构红染的梁状、带状或片状,失去纤维性结构。
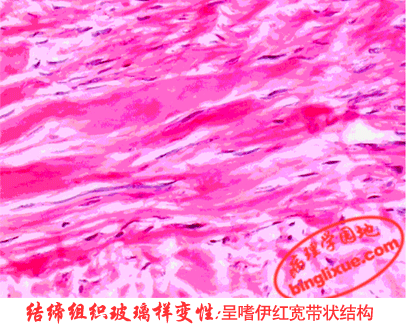
2. 血管壁的玻璃样变性
多发生于高血压病时的肾、脑、脾及视网膜的细小动脉。高血压病时,全身细小动脉持续痉挛,导致血管内膜缺血受损,通透性增高,血浆蛋白渗入内膜下,在内皮细胞下凝固,呈均匀、嗜伊红无结构的物质。使细小动脉管壁增厚、变硬,管腔狭窄、甚至闭塞,血流阻力增加,使血压升高,此即细动脉硬化症(arteriolosclerosis),可引起心、肾和脑的缺血。
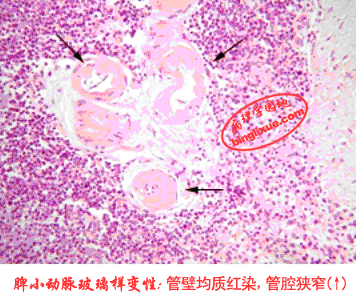
3. 细胞内玻璃样变性
细胞内玻璃样变性是指细胞内过多的蛋白质引起细胞发生了形态学改变。光镜下,常表现为圆形、嗜伊红的小体或团块。①肾小球肾炎或伴有明显蛋白尿的其他疾病时,肾脏近曲小管上皮细胞胞浆内,可出现大小不等的圆形红染小滴(玻璃小滴)。血浆蛋白经肾小球滤出,又被曲管上皮细胞吞饮并在胞浆内融合成玻璃样小滴。

(四) 粘液样变性
粘液样变性系指组织间质出现类粘液的聚集称为粘液样变性(mucoid degeneration)。肉眼所见:组织肿胀,切面灰白透明,似胶冻状。光镜下病变部位间质疏松,充以淡蓝色胶状物。其中,散在一些多角形或星芒状并以突起互相连缀的细胞。
结缔组织粘液样变性,常见于纤维瘤、平滑肌瘤等间叶性肿瘤,也可见于急性风湿病时心血管壁及动脉粥样硬化时的血管壁。甲状腺功能低下时,全身真皮及皮下组织的基质中,有类粘液及水分潴留,称为粘液性水肿(myxedema)。这可能是因为甲状腺素分泌减少,类粘液的主要成分透明质酸降解减弱所致。
一般认为,粘液样变性的结缔组织,当病因去除后,可逐渐恢复其形态与功能。但是严重而持久的粘液样变性,可引起纤维组织增生导致组织的硬化。
(五) 淀粉样变性
组织内有淀粉样物质(amyloid)沉着称为淀粉样变性(amyloid degeneration),亦称淀粉样物质沉着症(amyloidosis)。淀粉样物质是蛋白样物质,由于遇碘时,可被染成棕褐色,再加硫酸后呈蓝色,与淀粉遇碘时的反应相似,故称之为淀粉样变性。淀粉样物质常分布于细胞间或沉积在小血管的基底膜下,或者沿组织的网状纤维支架分布。病变为灰白色,质地较硬,富有弹性,光镜下HE切片中,淀粉样物质呈淡伊红染色、均匀一致、云雾状、无结构的物质。刚果红染色为橘红色,在偏光显微镜下呈黄绿色。电镜下,淀粉样物质为纤细的无分支的丝状纤维构成。
 |
淀粉样变性可为局部性的,也可为全身性的,其淀粉样物质生物化学本质也各不相同。与慢性炎症有关的局部性淀粉样变性多见于睑结膜、舌、喉、上呼吸道、肺、膀胱和皮肤等处,由于淀粉样物质沉着,局部形成结节,常伴有大量浆细胞等慢性炎细胞浸润。多发性骨髓瘤分泌的淀粉样物质为淀粉样轻链(amyloid light chain, AL)。与内分泌有关的局部性淀粉样变性发生在甲状腺髓样癌、胰岛细胞瘤、肾上腺嗜铬细胞瘤的间质内或Ⅱ型糖尿病患者的胰岛中,淀粉样物质内含有多肽激素或其他蛋白质。高龄老年人的心脏也可出现心脏内淀粉样物质沉着,引起心脏功能下降,称为老年性心脏淀粉样物质沉着症(senile heart amyloidosis),其沉着物质为淀粉样转甲状腺蛋白(amyloid transthyretin)。老年性大脑疾病如Alzheimer氏病脑组织中沉积物为β2淀粉样蛋白(beta2-amyloid protein)。全身性淀粉样变性可发生在长期慢性炎症疾病(结核病、支气管扩张症、慢性骨髓炎、类风湿性关节炎、畸形性脊椎炎、溃疡性结肠炎和Crohn病等)。这是由于炎症对组织和细胞的反复破坏引起的继发性病变,因而引起AA型(amyloid associated protein,AA)淀粉样物质沉着。家族性淀粉样变性也可表现为全身性病变。因肾衰竭而长期血液透析的患者的关节、肌腱和滑膜也可发生淀粉样变性,这是由于β2-微球蛋白(beta2-microglobulin)不能通过透析膜,在血液循环中维持高水平,并在关节、肌腱和滑膜等部位沉积引起的。
(六)细胞内糖原沉积
糖原是一种存在于细胞浆内的容易利用的储备能源。细胞内糖原沉积(intracellular accumulation of glycogen)发生于葡萄糖和糖原代谢异常的患者。糖原为水溶性,在非水溶性固定剂(如纯酒精)中保存较好。在一般HE染色切片中,糖原被溶去呈透明的泡状;PAS(periodic acid-schiff)染色中,呈玫瑰红色。细胞内糖原沉积常发生于糖尿病(diabetes mellitus)患者的近曲小管远端的上皮细胞内,甚至肝细胞、心肌细胞和胰岛β细胞内。患糖原沉着病(glycogen storage disease)时,由于患者糖原合成或降解的酶缺陷,也导致糖原在细胞内沉积。
(七)病理性色素
色素(pigments)是机体组织中的有色物质。有些色素是正常组织内存在的,如黑色素;有些色素是疾病状态下出现的,如肺内炭末颗粒沉着,称为病理性色素(pathological pigment)。根据来源不同,这些色素可分为内源性和外源性两类。内源性色素主要由机体细胞本身合成,如含铁血黄素、胆色素、脂褐素和黑色素等;外源性色素主要来自体外,如炭末、纹身的色素等。
(1)炭末
炭末(coal dust)来自体外,通过吸入到达人体肺部。肺内炭末沉积十分常见。多见于从事煤炭职业及过度吸烟人的肺部。肺组织内,可见大小不等的炭末颗粒,严重者,整个肺脏呈黑色。被吸入的炭末在肺内可被巨噬细胞吞噬,通过淋巴管引流,可沉积在肺间质及肺的淋巴结内。肺内严重的炭末沉积,可产生肺纤维化和肺气肿,引起严重的肺脏疾患。
(2)黑色素(melanin)
正常人皮肤、毛发、虹膜和脉络膜等处,均有黑色素存在。黑色素颗粒为棕褐色或深褐色,大小、形状不一。黑色素由黑色素细胞产生。在酪氨酸酶的作用下,黑色素细胞中的酪氨酸氧化为3,4-二羟苯丙氨酸(dihydroxyphenylalanine,DOPA),再进一步被氧化为吲哚醌。失去C02后,转化为二羟吲哚,后者形成一种不溶性的聚合物即为黑色素。黑色素细胞内因含有酪氨酸酶,故当加上多巴时,则出现与黑色素相似的物质,称多巴反应阳性;相反,表皮下吞噬了黑色素的组织细胞,因不含酪氨酸酶,故多巴反应阴性。用此方法可以鉴别黑色素细胞和噬黑色素细胞。ACTH分泌增多可致全身性皮肤黑色素增多。局限性黑色素增多则见于黑色素痣及黑色素瘤等。
 |
(3)脂褐素(lipofuscin)
是细胞内自噬溶酶体中的细胞器碎片发生某些理化反应后,不能被溶酶体酶消化而形成一种不溶性的黄褐色残存小体。多见于老年人及一些慢性消耗性疾病患者的心、肝和肾细胞内,故又有消耗性色素之称。
脂褐素也可见于正常人的附睾上皮细胞、睾丸间质细胞和神经细胞的胞浆中。光镜下,脂褐素呈黄褐色、颗粒状。电镜下:脂褐素颗粒呈典型的残存小体结构。脂褐素的主要生化成分为脂质和蛋白质。
(4)含铁血黄素(hemosiderin)
是由铁蛋白(ferritin)微粒集结而成的色素颗粒,呈金黄*色或棕黄*色,具有折光性。由于含铁血黄素分子中,含有三价铁,普鲁士蓝或柏林蓝反应呈蓝色。含铁血黄素是由血红蛋白被巨噬细胞溶酶体分解、转化而形成的。慢性肺淤血时,漏入肺泡腔内的红细胞,被巨噬细胞吞噬后,形成含铁血黄素。由于这种吞噬大量含铁血黄素的巨噬细胞常出现在左心衰竭患者,故此细胞又称心力衰竭细胞(heart failure cell)。此外,溶血性贫血时,可有大量红细胞被破坏,所以可出现全身性含铁血黄素沉积,常沉积于肝、脾、淋巴结和骨髓等器官组织内。
(八)病理性钙化
正常机体内,仅在骨和牙齿中含有固体钙盐。如果在骨和牙齿以外的其他组织内有固体钙盐沉积,则称之为病理性钙化(pathologic calcification)。沉积的钙盐主要是磷酸钙,其次为碳酸钙。组织内有少量钙盐沉积时,肉眼难以辨认;多量时,则表现为石灰样坚硬颗粒或团块状外观。HE染色切片中,钙盐呈蓝色颗粒状。起初,钙盐颗粒微细,以后可聚集成较大颗粒或团块。
 |
病理性钙化可分为营养不良性钙化和转移性钙化两种类型。
(1)营养不良性钙化
营养不良性钙化(dystrophic calcification)是指变性、坏死的组织或异物的钙盐沉积,较常见。而机体本身并无全身性钙、磷代谢障碍,血钙正常。此型钙化常发生在:结核坏死灶,脂肪坏死灶、动脉粥样硬化斑块,玻璃样变性或粘液样变性的结缔组织,坏死的寄生虫体、虫卵及其他异物等。
营养不良性钙化的发生机制尚不清楚。可能与局部碱性磷酸酶升高有关。此酶能水解有机磷酸酯,使局部磷酸超过3Ca2+:2P043-的正常值,所以形成磷酸钙沉积。至于磷酸酶的来源,一部分是从坏死细胞中的溶酶体释放出来的。还有一部分可能是吸收了周围组织液中的磷酸酶。此外,也有人认为,营养不良性钙化与变性、坏死组织的酸性环境有关。由于钙盐在酸性环境中易溶解,使局部钙离子浓度增高;随后由于组织液的缓冲,使局部碱性化,导致钙盐析出、沉积。
(2)转移性钙化
由于全身性的钙、磷代谢障碍,引起机体血钙或血磷升高,导致钙盐在未受损伤的组织内沉积,称为转移性钙化(metastatic calcification)。此种钙化较少见,多见于甲状旁腺功能亢进、过多接受维生素D或骨肿瘤造成骨组织严重破坏时,大量骨钙入血,血钙增高,使钙盐可沉积在全身许多未受损伤的组织中。常见的钙盐沉积部位有:肾小管,肺泡,胃粘膜等处。
病理性钙化对机体的影响:一般少量的钙盐沉积,有时可被溶解、吸收;当大量钙盐沉积时,则难以完全吸收,它可以作为一种异物长期存在于机体组织中,刺激周围纤维组织增生,将其包裹,并可在钙化的基础上发生骨化,对机体的影响依具体情况而有所不同。如:血管壁钙化后可以变硬、变脆,容易引起破裂出血;心瓣膜在变性、坏死基础上的钙化则可使瓣膜变硬、变形,从而引起血液动力学改变;结核病灶的钙化,可使其内的结核杆菌失去活力,使局部病变停止发展,病情处于相对稳定阶段。但是结核杆菌往往可在病灶中生活很长时间,一旦机体抵抗力低下时,疾病可能会复发。转移性钙化中,未受损伤的肾、肺、胃粘膜的钙盐沉积,可使这些组织本身功能下降甚至丧失。